Диагностика и лечение ранней стадии болезни Паркинсона
О.С. Левин1,2, А.В. Росинская3
1Российская медицинская академия последипломного образования; 2Центр экстрапирамидных заболеваний (Москва); 3Кабинет экстрапирамидных расстройств Приморской краевой клинической больницы №1 (Владивосток)
Болезнь Паркинсона (БП) – прогрессирующее нейродегенеративное заболевание, характеризующееся сочетанием гипокинезии с мышечной ригидностью и/или тремором покоя, а также с позднее развивающейся постуральной неустойчивостью и широким спектром немоторных нарушений, включая вегетативные, психические, диссомнические и сенсорные симптомы. В качестве основного звена патогенеза БП рассматривается формирование нейротоксических агрегатов небольшого пресинаптического белка альфа-синуклеина (основного компонента телец Леви) сопровождающееся гибелью пигментированных нейронов вентролатеральных отделов компактной части черной субстанции. Однако в последние годы установлено, что с поражением черной субстанции коррелируют лишь основные двигательные симптомы паркинсонизма, в то же время дегенеративный процесс при БП вовлекает и другие группы нейронов в различных зонах головного мозга, а также и в периферической нервной системе, что лежит в основе многочисленных немоторных проявлений болезни [1, 3].
Механизмы развития БП
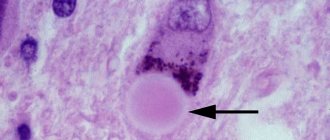
Это синуклеинопатия. При возникновении нейродегенеративных процессов внутри клеток постепенно накапливается альфа-синуклеиновый белок. Он получил название телец Леви. В начале заболевания тельца Леви можно обнаружить только в отделах периферической нервной системы. Они локализуются в сплетениях Мейснера и Ауэрбаха, расположенных в желудочно-кишечном тракте. При дальнейшем прогрессировании патологии тельца Леви «захватывают» ядра мозгового ствола и чёрную субстанцию продолговатого мозга.
Тяжёлые формы болезни Паркинсона характеризуются тем, что тельца Леви нарушают нормальные функции коры мозговых полушарий. При этом можно судить о топическом распространении нейродегенеративных изменений: пока чёрная субстанция не поражена, в клинической картине будут преобладать симптомы немоторного характера. По мере распространения патологии начинают гибнуть нигральные нейроны, что сопровождается появлением моторной симптоматики.
Эпидемиология
По данным сплошного популяционного исследования, распространенность БП в России составляет 139 случаев на 100 000 населения, заболеваемость БП – 16 случаев на 100 000 населения в год. С увеличением возраста риск БП увеличивается, и выявляемость БП среди лиц старше 65 лет составляет уже около 1%. Большинство случаев заболевания возникают в возрасте 60–70 лет. Однако в 15% случаев БП дебютирует в возрасте до 45 лет.
Исходя из имеющихся данных и половозрастной структуры населения России, можно примерно оценить общую численность больных с БП в нашей стране в 210 тысяч, при этом ежегодно заболевание возникает примерно у 20 тысяч пациентов. Ориентировочные расчеты показывают, что, как минимум, четверть пациентов (то есть более 50 тысяч) оказываются вне сферы медицинской помощи, причем в большинстве своем это пациенты с ранней стадией заболевания [3].
Диагностика
Диагноз БП проводится в 2 этапа. На первом (синдромальном) этапе синдром паркинсонизма требуется отличить от других состояний, имитирующих его (таблица 1).
Таблица 1. Состояния, требующие дифференциальной диагностики с паркинсонизмом.
| При наличии тремора | В отсутствие тремора |
| Усиленный физиологический тремор Эссенциальный тремор Дистонический тремор Гепатолентикулярная дегенерации | Апатико-абулический синдром Депрессия Лобная дисбазия Плечелопаточная периартропатия Гипотиреоз Шейный остехондроз Деменция с феноменом паратонии (противодержания) Кататония |
Ключевое значение в дифференциальной диагностике имеет выявление признаков гипокинезии. Начальные симптомы гипокинезии могут характеризоваться затруднениями при письме, нажатии кнопок на пульте, чистке зубов, печатании на клавиатуре, доставании мелких предметов, например, монет из сумки или кармана, надевании тапочек и т.д. Иногда уже на ранней стадии проявляется слабость и отставание одной из ног при ходьбе с изменением привычного рисунка походки. Характерно ослабление содружественных движений рук при ходьбе (ахейрокинез), нарушение подзарядки часов («симптом ролекса»). Могут обратить внимание ослабление голоса, замедление, ослабление интонирования или нечеткость речи (особенно при быстром произнесении морфологически сложных слов). При осмотре для выявления гипокинезии пациента просят выполнить определённые движения в течение примерно 20 секунд в максимально быстром темпе и с максимальной амплитудой. При этом врачу следует обращать внимание на замедленную инициацию движения, асимметрию движений, но главное – на особую форму истощаемости движений (декремент), которые по мере повторения все более замедляются, уменьшаются по амплитуде, требуют от пациента все больших усилий. Феномен истощаемости может выявляться при всех оцениваемых движениях, но иногда отмечается только в одном из тестов. Следует учитывать, что замедленность и неловкость движений, характерные для пациентов с паркинсонизмом, на ранней стадии можно спутать с проявлениями пирамидной и мозжечковой недостаточности, а также тяжелой депрессии, однако для этих состояний не характерен декремент движений по мере их повторения. Следует учитывать, что гипокинезию бывает трудно выявить на фоне грубого тремора в конечности, однако и в этом случае важно не пропустить диагностически значимый феномен: при паркинсонизме после выполнения теста на гипокинезию пациент часто держит руку в фиксированной напряженной позе и не способен быстро расслабиться.
Ригидность мышц проявляется устойчивым (в отличие от спастичности) сопротивлением пассивным движениям в лучезапястных, локтевых, плечевых, коленных суставах, а также в шее, а субъективно – скованностью и неприятными болезненными ощущениями в конечностях. У части пациентов при проверке тонуса выявляется феномен «зубчатого колеса». Следует отличать ригидность от феномена противодержания (gegenhalten), характерного для пациентов с деменцией и поражением лобных долей. Противодержание быстро меняется в зависимости от направления и скорости пассивного движения.
Медленный (3–4 Гц) тремор покоя в одной руке или ноге – одно из частых начальных проявлений паркинсонизма. Наличие классического тремора покоя по типу «скатывания пилюль» или «счета монет» наиболее характерно для БП. Для выявления латентного тремора пациента просят совершать движения другой рукой, походить, выполнить задачу на отвлечение (например, отнимать от 100 по 7). Для выявления тремора в ноге нужно осмотреть пациента в положении сидя или лежа. Вместе с тем, в отсутствие гипокинезии тремор покоя не позволяет диагностировать ни паркинсонизм, ни БП. Следует учитывать, что, с одной стороны, в покое может наблюдаться эссенциальный и дистонический тремор, с другой стороны, при БП часто наблюдается постуральный и кинетический тремор.
Начальным проявлением БП, особенно у лиц молодого возраста, может быть дистония стопы, появляющаяся или усиливающаяся при ходьбе, значительно реже – дистония иной локализации.
Ранние немоторные нарушения. Начиная с самой ранней (продромальной) стадии заболевания пациента могут беспокоить эмоциональная угнетенность, повышенная раздражительность, быстрая утомляемость или ощущение постоянной усталости, а также такие вегетативные нарушения, как расстройства потоотделения («дефектный термостат»), например, профузное потоотделение в холодную погоду, а также склонность к запорам, учащенные и/или императивные мочеиспускания, усиленное слюнотечение в ночное время (симптом «мокрой подушки»), эректильная дисфункция. Гипоосмия часто возникает уже на премоторной стадии БП, однако редко привлекает внимание самого пациента, и для ее выявления необходимо формализованное исследование (с помощью специальных методик, например, обонятельного теста Пенсильванского университета – UPSIT). Важное диагностическое значение может иметь выявление признаков синдрома нарушения поведения во сне с быстрыми движениями глаз (тревожные сновидения, вокализации, сноговорение, движения, отражающие содержание сновидений), которые могут опережать другие проявления заболевания на многие годы. Указанные немоторные проявления могут повышать точность диагноза, основывающегося на ранних моторных симптомах болезни.
Дебютными проявлениями БП бывают также хронические болевые синдромы, чаще всего в спине и плечелопаточной области, связанные с повышенным мышечным тонусом, ограничением мобильности и постуральными нарушениями.
Уже на ранней стадии могут выявляться признаки умеренного когнитивного расстройства, в частности неустойчивость внимания и замедленность мышления, трудности поиска слов (феномен «кончика языка»).
«Красные флажки». Второй этап – этап нозологической диагностики – сводится к дифференциальной диагностике БП с другими нозологическими формами паркинсонизма. Он требует клинической оценки анамнестических данных и данных, выявляемых при неврологическом осмотре. Важное значение имеет выяснение лекарственного анамнеза. Такие препараты, как метоклопрамид, вальпроат натрия, циннаризин, амиодарон, могут быть причиной лекарственного паркинсонизма. Отмена препарата, спровоцировавшего развитие паркинсонизма, может не приводить к немедленному регрессу симптомов. Иногда после о препарата и кратковременного улучшения состояние вновь ухудшается, что указывает на скрыто развивающийся дегенеративный процесс, который был «демаскирован» побочным действием лекарственных средств.
При неврологическом осмотре могут выявляться симптомы, атипичные для БП, требующие исключения иных заболеваний, вызывающих синдром паркинсонизма. Среди них можно выделить: симметричность, быстрое прогрессирование симптоматики с ранней утратой способности к передвижению в течние 5 лет, раннее развитие постуральной неустойчивости с падениями, отсутствие стойкого положительного эффекта адекватных доз препаратов леводопы, раннее развитие вегетативной недостаточности, быстрое присоединение деменции (в течении 1-го года), ограничение подвижности глазных яблок (особенно парез взора вниз), раннее развитие тяжелых псевдобульбарных синдромов, аксиальная дистония, пирамидные и мозжечковые знаки, наличие очаговых нарушений корковых функций.
Глава 13. Противопаркинсонические средства (Р.Н. Аляутдин)
Фармакология. Учебное пособие – под ред. Аляутдина Р.Н.
Противопаркинсонические средства — средства, применяемые для лечения болезни Паркинсона, синдрома паркинсонизма, включая лекарственный паркинсонизм.
Болезнь Паркинсона (дрожательный паралич) – хроническое нейродегенеративное заболевание, основой которого является поражение пигментсодержащих дофаминергических нейронов плотной части черной субстанции головного мозга. Основные клинические проявления болезни: брадикинезия (скованность движений), ригидность (повышенный тонус скелетных мышц) и тремор (дрожание) рук, головы. Клинические проявления болезни возникают при гибели 70-80% дофаминергических нейронов головного мозга. Болезнь Паркинсона (впервые была описана английским врачом Джеймсом Паркинсоном в 1817 г.) встречается у 1% населения в возрасте до 60 лет и у 5% – старше 60 лет. Возможной причиной заболевания является образование свободных кислородных радикалов в процессе окислительного метаболизма дофамина в черной субстанции мозга, что может вызвать разрушение дофаминергических нейронов. Имеются данные о том, что существует генетическая предрасположенность к болезни Паркинсона.
Причиной синдрома паркинсонизма, также проявляющегося дрожательным параличом, могут быть инфекционные заболевания нервной системы (вирусный энцефалит), сосудистые заболевания головного мозга, травмы черепа, интоксикации (оксидом углерода, марганцем, этанолом), сифилитические поражения мозга.
Лекарственный паркинсонизм – форма синдрома паркинсонизма, развивающаяся при длительном применении некоторых лекарственных средств, например, типичных нейролептиков (фенотиазины, бутирофеноны).
Паркинсонизм относят к экстрапирамидным расстройствам. Экстрапирамидная система, в частности хвостатое ядро и скорлупа, объединяемые в так называемый неостриатум, осуществляет корректировку и уточнение движений. Это достигается путем влияния на моторные зоны коры головного мозга через таламус. Активность холинергических нейронов неостриатума, контролирующих функции таламуса, тормозится дофаминергическими нейронами, расположенными в черной субстанции: аксоны дофаминергических нейронов черной субстанции оканчиваются в неостриатуме и выделяют дофамин, который стимулируя D2-peцепторы, расположенные на холинергических нейронах, оказывает на эти нейроны тормозное влияние (рис. 13.1). При болезни Паркинсона число дофаминергических нейронов уменьшается, что приводит к усилению холинергических влияний в неостриатуме и появлению характерных двигательных нарушений.
Кроме того, по некоторым данным активность холинергических нейронов контролируется глутаматергическими нейронами. Аксоны этих нейронов оканчиваются в неостриатуме и выделяют глутамат, который, стимулирует NMDA-рецепторы, расположенные на холинергических нейронах, и таким образом повышает их активность, в результате увеличивается выделение ацетилхолина в неостриатуме.
При болезни Паркинсона в связи с уменьшением тормозных дофаминергических влияний в неостриатуме начинают превалировать стимулирующие глутаматергические влияния и это приводит к большему повышению активности холинергических нейронов неостриатума и к развитию характерных симптомов заболевания. Для снятия этих симптомов необходимо восстановить нарушенный баланс между указанными системами в неостриатуме, что может быть достигнуто повышением дофаминергических влияний, снижением влияния глутаматергических нейронов, уменьшением влияния холинергических нейронов.
Рис. 13.1. Локализация действия противопаркинсонических средств. МАО-В – моноаминоксидаза В; D,-P – дофаминовые рецепторы.
D2–Постсинаптические дофаминовые рецепторы
В настоящее время при лечении болезни Паркинсона в основном используются следующие противопаркинсонические средства: Средства, стимулирующие дофаминергическую передачу Предшественник дофамина
Леводопа Ингибиторы моноаминоксидазы В
Селегилин (Депренил, Элдеприл, Юмекс) Средства, повышающие выделение дофамина
Амантадин (Мидантан) Средства, стимулирующие дофаминовые рецепторы (агонисты дофаминовых рецепторов)
Бромокриптин (Парлодел), перголид (Пермакс), прамипексол
(Мирапекс), ропинирол (Реквип) Средства, угнетающие холинергическую передачу
Центральные холиноблокаторы: Тригексифенидил (Циклодол), бипериден (Акинетон).
Средства, стимулирующие дофаминергическую передачу
Леводопа – левовращающий изомер диоксифенилаланина (L-ДОФА), непосредственный предшественник дофамина. Дофамин не проникает через гематоэнцефалический барьер. Леводопа проникает через гематоэнцефалический барьер путем активного транспорта (с помощью транспортной системы, которая переносит через мембраны ароматические аминокислоты). В неповрежденных дофаминергических нейронах леводопа под влиянием ДОФА-декарбоксилазы превращается в дофамин, который выделяется из окончаний дофаминергических волокон и стимулирует Д2-рецепторы на холинергических нейронах неостриатума (см. рис. 13.1). В результате активность этих нейронов снижается, что приводит к устранению симптомов паркинсонизма. Леводопа относится к наиболее эффективным противопаркинсоническим средствам: уменьшает брадикинезию, мышечную ригидность и в меньшей степени тремор.
Леводопа всасывается из кишечника путем активного транспорта, используя систему трансмембранного транспорта для ароматических аминокислот. Вследствие этого пища, богатая белками, способна снижать всасывание леводопы. В стенке кишечника и в печени леводопа подвергается интенсивному метаболизму под действием ДОФА-декарбоксилазы, что приводит к превращению в дофамин более 90% введенного препарата. Образовавшийся в периферических тканях дофамин не проникает в мозг и вызывает ряд побочных эффектов. Часть леводопы метаболизируется также МАО и КОМТ, в результате только 1—3% леводопы поступает в ЦНС.
Для предотвращения декарбоксилирования леводопы в периферических тканях используют ингибиторы ДОФА-декарбоксилазы, не проникающие через гематоэнцефалический барьер карбидопу и бенсеразид. При этом большее количество леводопы (около 10%) поступает в ткани мозга и достигает места своего действия. Это позволяет снизить назначаемую дозу леводопы. Кроме того, вследствие уменьшения образования дофамина в периферических тканях уменьшаются периферические побочные эффекты леводопы.
В настоящее время леводопа выпускается в комбинации с блокаторами периферической ДОФА-декарбоксилазы и входит в состав комбинированных
препаратов Наком, Синемет, Дуэллин (леводопа и карбидопа) и Мадопар (лево допа и бенсеразид).
Показаниями к назначению препаратов, содержащих леводопу, являются болезнь Паркинсона и паркинсонизм (за исключением лекарственного паркинсонизма). Принимают препараты внутрь только после еды. Леводопа хорошо всасывается из желудочно-кишечного тракта. Действие развивается медленно (через 1 нед) и достигает максимума через 1 мес. Лечение леводопой проводят длительно.
При применении леводопы возникают ортостатическая гипотензия, тахикардия, сердечные аритмии, которые связаны с образованием дофамина в периферических тканях и действием дофамина на сосуды и сердце. Кроме того, частыми побочными эффектами являются тошнота и рвота, которые возникают вследствие стимуляции дофамином D2– пусковой зоны рвотного центра. Эти эффекты уменьшаются при одновременном применении с леводопой ингибиторов периферической ДОФА-декарбоксилазы. Кроме того, для предупреждения тошноты и рвоты назначают блокатор дофаминовых рецепторов домперидон, который не проникает через гематоэнцефалический барьер, но действует на пусковую зону рвотного центра (пусковая зона рвотного центра не защищена гематоэнцефалическим барьером). При этом домперидон не блокирует дофаминовые рецепторы в неостриатуме и поэтому не снижает эффективность леводопы.
Такие побочные эффекты, как психозы, галлюцинации, бессонница, тревожность, депрессия, нарушение координации движений связаны с действием дофамина в ЦНС. Для устранения психозов применяют блокатор дофаминовых рецепторов центрального действия клозапин (атипичный нейролептик), который в большей степени блокирует D4-, чем Д2-рецепторы в ЦНС и поэтому в меньшей степени, чем типичные нейролептики влияет на эффективность леводопы.
У некоторых больных при длительном применении леводопы возникают дискинезии (непроизвольные хореиформные движения лица, шеи, конечностей). При длительном применении наблюдается синдром «включения/выключения», проявляющийся внезапным резким усилением симптомов болезни. Для уменьшения этого явления используют комбинированные препараты леводопы (леводопа+бенсеразид и леводопа+карбидопа) с замедленным высвобождением действующих веществ (Мадопар ГСС, Синимет-СР).
К противопоказаниям относят закрытоугольную глаукому, сахарный диабет, психозы, нарушения сердечного ритма, функции печени и почек, беременность, лактацию, возраст до 25 лет.
При длительном (более 5 лет) приеме леводопы эффективность снижается, что связано с прогрессирующей дегенерацией дофаминергических нейронов.
Для повышения эффективности леводопы, кроме ингибиторов ДОФА-декарбоксилазы, одновременно с леводопой назначают ингибиторы КОМТ. Одним из таких препаратов является энтакапон (Комтан). Препарат не проникает через гематоэнцефалический барьер и задерживает метаболизм леводопы в периферических тканях, при этом повышается количество леводопы, поступающей в ЦНС, что позволяет снизить дозу леводопы. Считается, что применение ингибиторов КОМТ уменьшает выраженность синдрома «включения/выключения».
Кроме того, для повышения эффективности проводимого лечения леводопу обычно сочетают с другими противопаркинсоническими средствами, которые улучшают дофаминергическую передачу. К ним относятся селегилин (ингибитор МАО-В), амантадин (препарат, высвобождающий дофамин из пресинаптических окончаний) и агонисты дофаминовых рецепторов.
Селегилин – селективный ингибитор МАО-В, фермента, который преимущественно инактивирует дофамин. Селегилин, угнетая МАО-В, уменьшает разрушение дофамина в нейронах черной субстанции (см. рис. 13.1) и потенцирует действие леводопы, что позволяет уменьшить дозу леводопы в среднем на 30%. Селегилин назначают в сочетании с леводопой. В качестве монотерапии препарат используют только на ранних стадиях болезни. Полагают, что селегилин обладает нейропротекторным действием, задерживая разрушение дофаминергических нейронов мозга. Этот эффект объясняют тем, что, угнетая окислительный метаболизм дофамина, селегелин уменьшает образование свободных кислородных радикалов, вызывающих гибель дофаминергических нейронов.
Побочные эффекты: тошнота, рвота, артериальная гипотензия, нарушение концентрации внимания и спутанность сознания.
Амантадин усиливает высвобождение дофамина из неповрежденных нейронов в синаптическую щель и нарушает обратный нейрональный захват дофамина (см. рис. 13.1). Повышение концентрации дофамина в ЦНС приводит к ослаблению симптомов болезни Паркинсона. Кроме того, не исключено взаимодействие амантадина с NMDA-рецепторами на холинергических нейронах базальных ядер. Полагают, что амантадин, блокируя эти рецепторы, препятствует стимулирующему действию глутамата на холинергические нейроны, что приводит к угнетению холинергической передачи в неостриатуме. Полагают также, что амантадин обладает некоторой антихолинергической активностью. Обсуждают нейропротекторный эффект амантадина в отношении дофаминергических нейронов черной субстанции, что связывают с блокадой NMDA-рецепторов, локализованных на этих нейронах. В результате уменьшается поступление в нервные клетки ионов кальция, что препятствует их разрушению.
Амантадин оказывает умеренный противопаркинсонический эффект. Применяют его при болезни Паркинсона и паркинсонизме (за исключением лекарственного паркинсонизма), в особенности при противопоказаниях к леводопе. Амантадин назначают также в сочетании с леводопой. К препарату быстро развивается привыкание.
К побочным эффектам относят возбуждение, раздражительность, бессонницу, головокружение, ортостатическую гипотензйю, судороги.
Агонисты дофаминовых рецепторов. В отличие от леводопы препараты этой группы непосредственно возбуждают дофаминовые рецепторы в неостриатуме (см. рис. 13.1). Неселективными агонистами D1- и Б2-рецепторов является перголид. Бромокриптин, прамипексол и ропинирол проявляют большую активность в отношении дофаминовых рецепторов Б2-класса (прамипексол и ропинирол стимулируют D2– и Б3-рецепторы этого класса). Перголид и бромокриптин относятся к производным алкалоидов спорыньи.
Бромокриптин является полусинтетическим производным алкалоида спорыньи эргокриптина. Противопаркинсоническая активность бромокриптина связана со стимуляцией Б2-рецепторов неостриатума. Кроме того, бромокриптин, стимулируя Б2-рецепторы, уменьшает высвобождение пролактина из передней доли гипофиза (см. раздел 31.1.1. «Препараты гормонов гипоталамуса и гипофиза»).
Бромокриптин и перголид в основном применяют в сочетании с леводопой, когда не удается получить удовлетворительных результатов, а также в случае возникновения синдрома «включения/выключения». Прамипексол и ропинирол по эффективности превосходят бромокриптин и назначаются как в виде монотерапии, так и в сочетании с леводопой. По продолжительности действия агонисты дофаминовых рецепторов превосходят леводопу.
В начале лечения агонистами дофаминовых рецепторов возникает ортостатическая гипотензия, тошнота, рвота (вследствие стимуляции Д2-рецепторов пусковой зоны рвотного центра), которые можно предупредить, назначая периферический блокатор дофаминовых рецепторов домперидон. При длительном применении возможны галлюцинации, психозы, развитие дискинезии. Для прамипексола и ропинирола, кроме того, характерны повышенная сонливость и внезапное засыпание.
Средства, угнетающие холинергическую передачу
Тригексифенидил – центральный холиноблокатор, блокируя М1-холинорецепторы неостриатума, уменьшает симптомы паркинсонизма. Препарат оказывает умеренное противопаркинсоническое действие. Преимущественно уменьшает тремор и мышечную ригидность, мало влияя на брадикинезию.
Бипериден — центральный холиноблокатор, близкий по свойствам тригексифенидилу.
Показания к назначению центральных холиноблокаторов: начальные стадии болезни Даркинсона и паркинсонизм. Применяют при лекарственном паркинсонизме, в частности, назначают для предупреждения и устранения экстрапирамидных расстройств, вызванных антипсихотическими средствами.
Побочные эффекты, связанные с блокадой периферических М-холинорецепторов: нарушение аккомодации, сухость во рту, сердцебиение, запоры, задержка мочеиспускания. Побочные эффекты, связанные с блокадой центральных М-холинорецепторов – нарушение памяти и концентрации внимания, особенно у пожилых пациентов. При передозировке возможны возбуждение, галлюцинации.
Противопоказания: глаукома, гипертрофия предстательной железы, гиперчувствительность к препарату, кормление грудью.
Взаимодействие противопаркинсонических средств с другими лекарственными средствами
| Противопаркинсонические средства | Взаимодействующий препарат (группа препаратов) | Результат взаимодействия |
| Леводопа | Бензодиазепины | Ослабление анксиолитического эффекта |
| Ингаляционные средства для наркоза | Повышение риска аритмии сердца | |
| Ингибиторы МАО | Повышение артериального давления | |
| Антигипертензивные средства | Потенцирование гипотензивного эффекта | |
| Препараты железа | Снижение всасывания железа | |
| Метоклопрамид | Повышение плазменной концентрации и токсичности леводопы | |
| Селегилин | Повышение риска дискинезии, тошноты, ортостатической гипотензии, галлюцинаций | |
| Пиридоксин | Активация ДОФА-декарбоксилазы, снижение концентрации леводопы | |
| Бромокриптин | Антибиотики – макролиды | Повышение плазменной концентрации бромокриптина |
| Метоклопрамид, Домперидон | Уменьшение гипопролактинемии, вызываемой бромокриптином | |
| Антипсихотические средства | Антагонизм с гипопролактинемическим и антипаркинсоническим эффектами бромокриптина | |
| Тригексифенидил, Бипериден | Холиноблокаторы и другие препараты с холиноблокирующей активностью | Потенцирование холиноблокирующего действия |
Основные препараты
| Международное непатентованное название | Патентованные (торговые) названия | Формы выпуска | Информация для пациента |
| Леводопа (Levodopa) | Наком, Сине-мет, Дуэллин (леводопа+кар-бидопа), Мадо-пар (леводопа+ бенсеразид) | Таблетки по 0,1, 0,125, 0,15, 0,2 и 0,25 г леводопы | Применяется внутрь, начальная доза – 125 мг леводопы 3-4 раза в день, суточная – 750 мг-1,5 г в несколько приемов после еды |
| Селегилин (Selegilinum) | Депренил, Элдеприл, Юмекс | Таблетки по 0,005 г в упаковке 50 и 1000 шт. | Принимают внутрь, начиная с 5 мг утром (вместе с завтраком); если нет результата — дозу увеличивают до 10 мгв день |
| Амантадин (Amantadinum) | Мидантан | Таблетки по 0,1 г в упаковке 100 шт. | Принимают внутрь, после еды, начиная с 50-100 мг 2 раза, затем -3—4 раза в день. Суточная доза — 200-400 мг. Курс – 2-4 мес |
| Бромокриптин (Bromocripti- num) | Парлодел | Таблетки по 0,0025 г бромокриптина моно-сульфоната во флаконах по 100, 500 или 1000 шт. | Принимают внутрь во время еды — начальная доза 1,25 мг перед сном с последующим увеличением через 2-3 дня до 1,25 мг 2 раза в день. При необходимости дозу увеличивают каждые 2—4 нед на 2,5 мг в сутки. Средняя эффективная доза составляет 10 мг, максимальная — 40 мг/сут. Несовместим с алкоголем |
| Тригексифени-дил (Trihexyphe-nidylum) | Циклодол | Таблетки по 0,002 г в упаковке по 50 шт. | Принимают внутрь, начиная с 10 мг/сут; увеличивая дозу по 2 мг/сут. Обычная поддерживающая суточная доза – 6-10 мг (для пожилых — меньше), в тяжелых случаях – 12-15 мг/сут в 3-4 приема. Высшие дозы: разовая -10 мг, суточная – 20 мг |
Дополнительные методы исследования
В настоящий момент нет методов лабораторного или инструментального исследования, которые были бы обязательны у каждого пациента с подозрением на БП. В последние годы больным с БП часто проводят КТ или МРТ головного мозга, однако чаще всего в этом нет необходимости, и в большинстве случаев диагноз может быть установлен на основе клинических данных. Тем не менее, если клиническая картина у больного с синдромом паркинсонизма отклоняется от классического варианта, свойственного БП, в частности, отсутствует типичная реакция на дофаминергические средства, – необходимо проведение нейровизуализации.
При начале заболевания до 50 лет важно исключить гепатолентикулярную дегенерацию, о которой могут свидетельствовать роговичное кольцо Кайзера–Флейшера, низкий уровень церулоплазмина, повышение интенсивности сигнала от базальных ганглиев и мозжечка на Т2-взвешенных МРТ изображениях, повышенная экскреция меди с мочой.
Диагностическую значимость может иметь и транскраниальная сонография глубинных структур мозга, выявляющее при БП гиперэхогенные изменения в проекции черной субстанции, связанные с накоплением железа и установленные в 92% случаев клинически вероятной БП, однако его результаты можно интерпретировать лишь в клиническом контексте.
Из практически важных, но пока отсутствующих в нашей стране, методов диагностики следует упомянуть позитронно-эмиссионную томографию (ПЭТ) и однофотонную эмиссионную компьютерную томографию (ОФЭКТ), позволяющие изучить синаптическую передачу на всех уровнях, а также проводить мониторинг патологического процесса. При выявлении снижение накопления F18-флюородопы при ПЭТ и β-CIT при ОФЭКТ в полосатом теле можно говорить о вовлечении в патологический процесс пресинаптических нигростриарных терминалей (первичный паркинсонизм). Определение снижение накопления 11С-раклоприда (лиганд D2рецепторов) при ПЭТ будет указывать на уменьшение количества дофаминовых рецепторов в полосатом теле (паркинсонизм «плюс»).
Общие принципы начала лечения
Поскольку на данный момент способность замедлять процесс дегенерации за счет нейропротективного эффекта (возможность защищать интактные клетки от повреждения) или нейрорепаративного эффекта (возможность восстанавливать активность частично поврежденных клеток) ни у одного из применяющихся средств убедительно не доказана, лечение основывается пока на симптоматическом действии. Тем не менее потенциальная возможность нейропротективного эффекта, подтверждаемая экспериментальными или клиническими данными, должна учитываться при назначении лечения.
В настоящее время широкое распространение получила концепция, подчеркивающая важность раннего назначения дофаминергической терапии – немедленно после установления диагноза – с тем, чтобы быстрее скорректировать нейрохимический дисбаланс в мозге и поддержать процессы компенсации.
Если ранее подчеркивалась необходимость возможно более длительного сохранения монотерапии, то в настоящее время преимущества такого подхода не представляются очевидными – по сравнению с ранним переходом к комбинации средств с разным механизмом действия. Вопрос о необходимости монотерапии или комбинированной терапии должен решаться индивидуально. В любом случае при выборе препаратов и их дозы следует стремиться не к полному устранению симптомов, а к существенному улучшению функций, позволяющему поддерживать бытовую и профессиональную активность. В то же время следует избегать внесения в схему лечения сразу нескольких изменений (например, повышения дозы сразу нескольких средств или добавления сразу нескольких препаратов), это позволяет оценить отдельно эффективность и безопасность каждого из назначаемых средств.
Принципы выбора противопаркинсонического препарата
Выбор препарата на начальном этапе лечения проводят с учетом возраста, выраженности двигательного дефекта, трудового статуса, состояния нейропсихологических функций, наличия сопутствующих соматических заболеваний, индивидуальной чувствительности пациента. Помимо достижения оптимального симптоматического контроля, выбор препарата определяется необходимостью отсрочить момент развития моторных флуктуаций и дискинезий (таблица 2).
Таблица 2. Выбор препарата для начального лечения болезни Паркинсона.
| Препараты | Возможность использования в качестве средства первого выбора | Степень симптоматического улучшения | Нейро-протективный потенциал | Риск побочного действия | |
| Флуктуации и дискинезии | Другие побочные эффекты | ||||
| Леводопа | + | +++ | +? | ↑ | ↑ |
| Агонисты дофаминовых рецепторов | + | ++ | +? | ↓ | ↑ |
| Ингибитор МАО В | + | + | +? | ↓ | ↑ |
| Амантадин | + | + | +? | ↓ | ↑ |
| Холинолитики | — | + | — | ? | ↑ |
У лиц моложе 50 лет при легкой или умеренной выраженности двигательных нарушений в отсутствие выраженных когнитивных нарушений назначают один из следующих препаратов: агонист дофаминовых рецепторов, ингибитор моноаминооксидазы типа В, амантадин. При более легком двигательном дефекте может быть назначен ингибитор МАО В, при более выраженном дефекте предпочтительнее начинать с лечения с одного из агонистов дофаминовых рецепторов. Неэрголиновые агонисты (например, прамипексол, ропинирол, ротиготин или проноран) ввиду более благоприятного профиля побочных эффектов предпочтительнее, чем эрголиновые (бромокриптин, каберголин). При недостаточной эффективности или плохой переносимости одного из агонистов дофаминовых рецепторов может быть испробован другой агонист дофаминовых рецепторов или препарат другой фармакологической группы. Рациональна комбинация агониста дофаминовых рецепторов, ингибитора МАО типа В и амантадина, к которой следует переходить постепенно, добавляя препарат новой группы, если ранее назначенное средство не обеспечило ожидаемого эффекта.
Антихолинергические средства (например, бипериден) показаны при наличии выраженного тремора покоя либо болезненной дистонии при условии сохранности нейропсихологических функций. Их целесообразно добавлять к комбинации агониста дофаминовых рецепторов с ингибитором МАО В и/или амантадином, если она у пациента относительно молодого возраста не обеспечила подавления тремора в той степени, в которой это необходимо для поддержания его трудоспособности.
Если указанные препараты в максимально переносимых дозах и их комбинация не обеспечивают адекватного состояния двигательных функций и социальной адаптации больных, назначают препарат леводопы в минимальной эффективной дозе [4].
У лиц в возрасте 50–70 лет при умеренном двигательном дефекте и относительной сохранности когнитивных функций лечение начинают с ингибитора МАО типа В (при легких симптомах паркинсонизма) или одного из агонистов дофаминовых рецепторов. В дальнейшем целесообразен постепенный переход к комбинации агониста дофаминовых рецепторов, ингибитора МАО типа В и амантадина (при условии хорошей переносимости). Больным после 60 лет антихолинергические средства, как правило, не следует назначать из-за риска ухудшения познавательных функций и других побочных эффектов. При недостаточной эффективности комбинации указанных выше препаратов добавляют препарат леводопы в минимальной эффективной дозе (200–400 мг в сутки).
У лиц в возрасте 50–70 лет при выраженном двигательном дефекте, ограничивающем трудоспособность и(или) возможность самообслуживания, а также при наличии выраженных когнитивных нарушений и необходимости получения быстрого эффекта лечение начинают с препаратов, содержащих леводопу. Если небольшие или средние дозы леводопы (300–500 мг леводопы в сутки) не обеспечивают необходимого улучшения, к ним последовательно могут быть добавлены агонист дофаминовых рецепторов, амантадин и ингибитор МАО В.
У пожилых лиц (старше 70 лет), особенно при наличии выраженного когнитивного снижения и соматической отягощенности, лечение следует начинать с препаратов леводопы. Указанные возрастные границы относительны, и общий принцип скорее заключается в том, что чем моложе больной, тем позже следует вводить препараты леводопы. Кроме того, решающее значение играет не столько хронологический, сколько биологический возраст больных.
Правила назначения и побочные эффекты препаратов противопаркинсонического действия
Поскольку речь идёт о специфических препаратах и их комбинациях, важно учитывать несколько моментов:
- клиническое течение и степень тяжести симптоматики;
- степень эффективности каждого лекарства при приёме у конкретного пациента;
- наличие или отсутствие побочных действий.
Если болезнь Паркинсона началась в относительно молодом возрасте (до 50-летнего рубежа), первый препарат, который стоит рассматривать для назначения, — это антагонист дофаминовых рецепторов. При позднем развитии заболевания (в возрасте от 70 лет и старше) предпочтение нужно отдавать препаратам леводопы.
Безусловно, леводопу необходимо рассматривать в качестве некого «золотого стандарта», но, к сожалению, она всегда даёт ряд осложнений в виде колебаний её эффекта и расстройств моторики. Вначале больной ощущает, как заканчивается действие препарата, а позже у него появляются феномены «включения-выключения». При появлении моторных флюктуаций у больных могут возникнуть побочные явления со стороны психической, вегетативной и сенсорной сфер. Также следует учитывать и феномен так называемой лекарственной дискинезии, когда у человека наблюдается ряд странных насильственных движений, которые он не может контролировать. Как правило, этот феномен возникает на поздних стадиях болезни и означает пик действия лекарственного препарата.
При тяжёлых осложнениях, связанных с использованием леводопы, рекомендуется прибегать к способам, которые позволяют стимулировать рецепторы дофамина в организме. Речь идёт о введении геля на основе леводопы путём гастростомы. Также допускается подкожное введение апоморфина.
Если приходится прибегать к интрадуоденальному введению препарата, нужно периодически показывать больного хирургу, чтобы избежать типичных осложнений. Введение апоморфина подкожно является более щадящим вариантом терапии, хотя побочные эффекты есть и в данном случае.
Применение препарата прамипексола с длительным высвобождением на ранней стадии БП
Разработка новых лекарственных форм противопаркинсонических препаратов, обеспечивающих их длительное высвобождение и допускающих однократный прием в течение дня, не просто делает лечение более удобным, но и, улучшая приверженность пациентов лечению, повышает долгосрочную эффективность терапии. Кроме того, при медленном высвобождении препарата в течение суток достигается более стабильная его концентрация в крови, что может обеспечить его лучшую переносимость и эффективный контроль симптомов заболевания в течение всего дня (как в дневное, так и в ночное время).
Новая лекарственная форма прамипексола с длительным (контролируемым) высвобождением, предполагающая однократный прием в течение дня, применяется в европейских странах и США с 2009 года, а в нашей стране – с 2012 года. Она представляет собой матриксную таблетку, в которой активное вещество равномерно распределено в полимерном матриксе. В желудочно-кишечном тракте матрикс впитывает жидкость и превращается в гель, который равномерно высвобождает прамипексол в течение 24 ч. Поскольку прамипексол хорошо растворяется в жидкой среде, независимо от ее pH, активное вещество высвобождается из матрикса и всасывается на протяжении всего кишечника. Скорость опорожнения желудка и моторика кишечника не оказывают существенного влияния на действие препарата. Параметры всасывания не зависят также от того, принимается препарат натощак или после еды [2].
При разработке новой лекарственной формы была учтена возможность простого, одномоментного перехода от традиционной формы препарата к новой. Условием этого является то, что равные суточные дозы препарата с немедленным высвобождением (принимаемым 3 раза в день) и длительным высвобождение (принимаемым 1 раз в день) оказывают одинаковое противопаркинсоническое действие. Различие между новой и традиционной лекарственными формами прамипексола заключается лишь в скорости высвобождения активного вещества. Период полужизни прамипексола при применении обеих форм один и тот же, но благодаря контролируемому высвобождению обеспечивается более длительное поддержание терапевтической концентрации препарата в крови [5].
Эквивалентность действия равных суточных доз препаратов прамипексола с немедленным и длительным высвобождением была подтверждена в целом ряде клинических испытаний.
Следует подчеркнуть особое удобство новой лекарственной формы прамипексола, которую достаточно принимать один раз в день, для пациентов с ранней стадией БП, продолжающих работать. Во избежание побочного действия препарат назначается путем медленного титрования – по той же схеме, что и препарат с немедленным высвобождением. Для этого таблетки прамипексола с длительным высвобождением выпускаются в нескольких дозировках: 0,375, 0,75, 1,5, 3 и 4,5 мг. Лечение начинают с дозы 0,375 мг 1 раз в день, далее при условии хорошей переносимости каждые 7 дней переходят на следующий уровень дозы до достижения оптимального эффекта, максимально до 4,5 мг/сут (таблица 3). После достижения дозы 1,5 мг/сут титрование иногда целесообразно проводить медленнее, так как развитие полного лечебного эффекта может требовать нескольких недель. Рекомендуемая доза для поддерживающей терапии (как на ранней, так и на развернутой или поздней стадиях заболевания) может колебаться от 0,375 до 4,5 мг/сут. Наиболее часто применяемая доза – 3 мг/сут.
Таблица 3. Схема титрования прамипексола с длительным высвобождением.
| Неделя | Доза |
| 1-я | 0,375 мг 1 раз в день |
| 2-я | 0,75 мг 1 раз в день |
| 3-я | 1,5 мг 1 раз в день |
| 4-я | 2,25 мг 1 раз в день |
| 5-я | 3 мг 1 раз в день |
| 6-я | 3,75 мг 1 раз в день |
| 7-я | 4,5 мг 1 раз в день |
Стандарты лечения болезни Паркинсона
Лечение при появлении моторных флуктуаций и/или дискинезий
Уменьшение длительности действия средств, содержащих леводопу.
При усилении симптомов паркинсонизма к концу действия очередной дозы средства, содержащего леводопу, прибегают к одной из следующих мер:
- увеличение кратности приема средства, содержащего леводопу, до 4–6 раз при сохранении неизменной суточной дозы или ее минимальном увеличении (уровень доказательности С);
- частичная замена стандартного препарата, содержащего леводопу, на препарат, содержащий леводопу, с замедленным высвобождением (уровень В);
- добавление одного из агонистов дофаминовых рецепторов — прамипексола, пирибедила или бромокриптина (уровень В);
- добавление ингибитора МАО типа В селегилина или амантадина (уровень С);
- добавление ингибитора катехол-О-метилтрансферазы (КОМТ) энтакапона или толкапона (уровень А).
Если выбранная мера оказалась неэффективной, следует применить комбинацию препаратов (уровень С).
Замедленное наступление или отсутствие эффекта разовой дозы средства, содержащего леводопу.
Если отдельные дозы препарата леводопы, принятые в течение дня, оказываются неэффективными, рекомендуют:
- прием препарата, содержащего леводопу, на пустой желудок (не менее чем за 45 мин до приема пищи) (уровень С);
- прием препарата леводопы в растворенном виде (уровень С);
- назначение препаратов, усиливающих моторику желудка — например, домперидона (уровень С).
Непредсказуемые колебания эффекта разовой дозы средств, содержащих леводопу, в течение дня (синдром «включения-выключения»).
При появлении эпизодов внезапного усиления симптомов паркинсонизма на фоне действия очередной дозы леводопы следует предпринять следующее:
- оценить адекватность доз леводопы (излишне малые дозы не обеспечивают полноценного длительного эффекта) (уровень С);
- увеличить разовую дозу леводопы, продлив интервал между приемами препарата до 4–5 ч (уровень С);
- добавить один из агонистов дофаминовых рецепторов (уровень В);
- принимать средство, содержащее леводопу, за 45–60 мин до еды, ограничить употребление белков в дневное время, назначить препараты, усиливающие моторику желудочно-кишечного тракта (домперидон) (уровень С);
- при затянувшемся выключении принимают препарат леводопы в растворенном виде (уровень С).
Кроме того, показаны меры, аналогичные рекомендуемым, при замедленном наступлении или отсутствии эффекта разовой дозы средства, содержащего леводопу.
Насильственные движения на высоте действия разовой дозы средства, содержащего леводопу (дискинезия пика дозы).
Если на высоте действия препарата леводопы появляются насильственные движения, ограничивающие жизнедеятельность пациента, нужно предпринять следующие действия:
- добавить амантадин (уровень А);
- снизить разовую дозу леводопы, компенсировав это увеличением числа приемов, добавлением или увеличением дозы агониста дофаминовых рецепторов (уровень С);
- снизить дозу или отменить селегилин, ингибитор КОМТ и антихолинергическое средство (уровень С);
- частично заменить стандартное средство, содержащее леводопу, на средство с замедленным высвобождением (при этом возможно увеличение длительности насильственных движений, что требует отмены препарата с замедленным высвобождением) (уровень С);
- добавить клоназепам (уровень С);
- добавить клозапин (в наиболее тяжелых случаях) (уровень С).
Насильственные движения в начале и конце действия разовой дозы средства, содержащего леводопу (двухфазные дискинезии).
При двухфазных дискинезиях нужно предпринять следующие меры:
- увеличить разовую дозу леводопы, при необходимости уменьшив число приемов (очередная доза должна быть принята не ранее, чем будет завершен полный цикл дискинезий) (уровень С);
- добавить один из агонистов дофаминовых рецепторов, сохраняя или уменьшая дозу леводопы (уровень С);
- отменить средство, содержащее леводопу, с замедленным высвобождением (уровень С).
Дистония, вызванная прекращением действия очередной дозы средства, содержащего леводопу.
При болезненных дистониях, вызываемых прекращением действия очередной дозы средства, содержащего леводопу, необходимы следующие меры:
- увеличение числа приемов средства, содержащего леводопу (уровень С);
- добавление средства, содержащего леводопу, с замедленным высвобождением или частичная замена стандартного средства препаратом с замедленным высвобождением (уровень В);
- добавление одного из агонистов дофаминовых рецепторов (уровень В);
- прием средства, содержащего леводопу, в растворенном виде (уровень В);
- дополнительное назначение антихолинергического средства (в отсутствие нарушения познавательных функций), баклофена, клоназепама, тизанидина, препарата лития или инъекции ботулотоксина в мышцы, вовлеченные в гиперкинез (уровень С).
Если, несмотря на коррекцию схемы приема противопаркинсонических средств, сохраняются непроизвольные движения или нестабильность эффекта средств, содержащих леводопу, которые существенно ограничивают жизнедеятельность пациента (снижают трудоспособность или возможность самообслуживания), показана консультация нейрохирурга, специализирующегося в стереотаксической нейрохирургии, для решения вопроса о целесообразности нейрохирургического вмешательства.
Лечение нарушений сна
При пробуждениях, вызванных усилением симптомов паркинсонизма в ночное время (ночная акинезия), прибегают к одной из следующих мер:
- увеличение вечерней дозы средства, содержащего леводопу (уровень В);
- замена в вечерний прием стандартного препарата леводопы средством с замедленным высвобождением (уровень С);
- назначение агониста дофаминовых рецепторов непосредственно перед сном (уровень С).
При ночной акатизии уменьшают вечернюю дозу средства, содержащего леводопу (уровень С), а если эта мера оказывается недостаточной, то на ночь назначают клоназепам (уровень С). При неэффективности указанных мер дополнительно назначают золпидем, 10–20 мг на ночь (уровень С), антидепрессант с седативным действием (тразодон — 75–150 мг, амитриптилин — 25–50 мг или миртазапин — 15–30 мг) (уровень С).
Лечение больных БП с нарушением познавательных функций
Ухудшение познавательных функций требует в первую очередь оптимизации противопаркинсонической терапии с обеспечением адекватного уровня двигательных функций. Основным противопаркинсоническим средством у больных с выраженными познавательными нарушениями должны быть препараты, содержащие леводопу, которые у этой категории больных реже вызывают побочные эффекты (уровень С). Назначение антихолинергических средств противопоказано в связи с высоким риском ухудшения психических функций и развития психотических расстройств (уровень В).
Кроме того, при ухудшении познавательных функций необходимы:
- выявление и коррекция сопутствующих заболеваний, способных ухудшить психический статус (интеркуррентные инфекции, гипотиреоз, соматические заболевания и др.);
- отмена препаратов, способных усилить познавательные нарушения (в том числе средств с антихолинергическим действием, бензодиазепинов и т. д.);
- после консультации психиатра — коррекция аффективных нарушений с помощью антидепрессантов, не оказывающих холинолитического или седативного действия, предпочтительнее с помощью селективных ингибиторов обратного захвата серотонина со стимулирующим эффектом, в частности циталопрама, сертралина или флуоксетина (необходим регулярный клинический контроль в связи с возможным ухудшением двигательных функций).
Для улучшения познавательных функций у больных БП с деменцией могут применяться:
- ингибиторы центральной холинэстеразы: ривастигмин, 3–12 мг/сут в 2 приема (уровень А), галантамин, 8–24 мг/сут в 2 приема (уровень С);
- блокатор NMDA-глутаматных рецепторов мемантин, 10–30 мг в 1–2 приема (уровень С).
Консультация психиатра и наблюдение за больными с психическими нарушениями показаны при развитии тяжелых психотических расстройств (депрессии, психопатоподобные нарушения, галлюциноз, параноидный синдром, делирий).
При зрительных галлюцинациях на фоне ясного сознания, сохранности ориентации и критики проводится плановая коррекция противопаркинсонической терапии (уровень В). В первую очередь снижают дозу или отменяют недавно назначенное или наименее эффективное средство (уровень В), часто в следующем порядке: холинолитик — селегилин — амантадин — агонист дофаминовых рецепторов — ингибитор КОМТ (уровень С).
При сохранении галлюцинаций следует снизить дозу средства, содержащего леводопу, до минимального эффективного уровня, обеспечивающего необходимый уровень двигательной активности (уровень В). При неэффективности этой меры или невозможности снизить дозу средства, содержащего леводопу, из-за нарастания двигательного дефекта назначается клозапин в дозе от 6,25 до 50 мг на ночь (уровень В); после регресса галлюциноза препарат постепенно отменяют в течение 2–3 нед (уровень С). В течение всего срока лечения клозапином необходимо 1 раз в неделю исследовать содержание лейкоцитов в крови. При снижении их уровня ниже 3 тыс./мкл препарат должен быть отменен.
При неэффективности или непереносимости клозапина вместо него может быть назначен кветиапин, 25–200 мг/сут (уровень С), ингибитор холинэстеразы (уровень С).
При сочетании зрительных галлюцинаций с бредовыми нарушениями или при их возникновении на фоне спутанности сознания с развитием делирия необходимо, помимо указанных выше мер, следующее:
- организовать постоянное наблюдение за больным;
- выявить провоцирующие факторы — инфекция, травма, соматические и цереброваскулярные заболевания и др. — и начать их лечение;
- уменьшить дозу или постепенно отменить препараты, прием которых мог явиться причиной психотических нарушений (холинолитики, селегилин, амантадин, агонист дофаминовых рецепторов, ингибитор КОМТ);
- снизить дозу препарата леводопы до минимального эффективного уровня и обеспечить контроль за ее регулярным приемом;
- организовать консультацию психиатра и рассмотреть вопрос о госпитализации в психосоматическое отделение.
Следует избегать назначения на ночь бензодиазепинов с длительным действием (диазепам, хлордиазепоксид и т. д.), способных спровоцировать спутанность сознания.
Лечение акинетического криза
Акинетический криз — внезапное стойкое усиление гипокинезии и ригидности с развитием обездвиженности и нарушения бульбарных функций (дизартрии и дисфагии), возникающее спонтанно или связанное с прекращением приема, снижением дозы средств, содержащих леводопу, нарушением их всасывания в желудочно-кишечном тракте, развитием интеркуррентной инфекции.
Лечение осуществляется в условиях стационара. Проводится исследование причин акинетического криза (прекращение приема или снижение дозы противопаркинсонических средств, заболевание желудочно-кишечного тракта, вызывающее нарушение всасывания препаратов леводопы, интеркуррентная инфекция, цереброваскулярное заболевание, декомпенсация соматического заболевания).
Лекарственная терапия назначается индивидуально на основании данных анамнеза и ежедневного осмотра пациента. При дисфагии необходимо введение назогастрального зонда для кормления и введения лекарств. Показан комплекс мер по предупреждению пролежней, прежде всего повороты в постели каждые 2 ч, регулярная обработка мест костных выступов камфорным спиртом, использование противопролежневых матрасов.
Если акинетический криз возник в результате внезапного прекращения приема средства, содержащего леводопу, то его следует назначить вновь в более низкой дозе (50–100 мг 3–4 раза в сутки), затем постепенно увеличивать дозу каждые 3 дня до получения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
Если акинетический криз возник вследствие снижения дозы, то ее следует увеличить на 100 мг каждые 3 сут до достижения эффекта (но не более чем до 700–800 мг леводопы в сутки) (уровень С).
При дисфагии (но при нормальной функции желудочно-кишечного тракта) препараты леводопы вводят в растворенном виде через зонд.
В качестве дополнительного средства, особенно при нарушении глотания и всасывания препаратов в желудочно-кишечном тракте, назначают амантадина сульфат — 200 мг/500 мл в/в капельно со скоростью 60 капель в 1 мин 1–2 раза в сутки в течение 5–10 дней (уровень С) с последующим обязательным переходом на прием амантадина внутрь (100–200 мг 3 раза в день).
При дегидратации с целью достижения эуволемии вводят физиологический раствор, раствор Рингера, 0,45% раствор хлорида натрия и 5% раствор глюкозы, раствор альбумина, Реополиглюкин (уровень С).
Для профилактики тромбоза глубоких вен голени и тромбоэмболических осложнений показано назначение прямых антикоагулянтов (Гепарин, 2,5–5 тыс. единиц подкожно 2 раза в день или Фраксипарин 0,3 мл подкожно 2 раза в сутки) до разрешения акинетического криза (уровень С).
До восстановления глотания питание проводится через назогастральный зонд. При нарушении функции желудочно-кишечного тракта проводится парентеральное питание.
При появлении дыхательной недостаточности, острой сердечной недостаточности и тяжелой дисфагии, создающей угрозу аспирации, больной переводится в отделение интенсивной терапии, где проводится интубация, а при необходимости и искусственная вентиляция легких. Реабилитация, включающая лечебную гимнастику и массаж, осуществляется после купирования криза и стабилизации состояния.
По вопросам литературы обращайтесь в редакцию.
О. С. Левин,
доктор медицинских наук, профессорРМАПО, Центр экстрапирамидных заболеваний,Москва
Продолжение. Начало см.: Лечащий врач. 2007. №8
Лекарственные средства, эффективность которых при БП не доказана
В клинической практике широко применяют лекарственные средства, эффективность которых при БП не доказана и которые, следовательно, не могут быть рекомендованы к применению при этом заболевании. Прежде всего, к ним относятся так называемые ноотропные, нейрометаболические и вазоактивные препараты. Возможно, некоторые из этих средств оказывают определенное лечебное действие, но прежде, чем рекомендовать конкретный препарат, следует провести адекватную оценку его эффективности. Специалисты, занимающиеся лечением БП, прекрасно знают, что определенная часть больных хорошо реагирует на плацебо, причем этот эффект оказывается нестойким. Соответственно, затраты на подобное лечение оказываются бессмысленными.
Литература
- Голубев В.Л., Левин Я.И., Вейн А.М. Болезнь Паркинсона и синдром паркинсонизма. М.: МЕДпресс-информ, 1999.
- Левин О.С., Федорова Н.В., Смоленцева И.Г. Агонисты дофаминовых рецепторов в лечении болезни Паркинсона. Рус. мед. журн. 2000; 15–16: 643–646.
- Левин О.С., Федорова Н.В. Болезнь Паркинсона. М.: МЕДпресс-информ, 2011.
- Протокол ведения больных. Болезнь Паркинсона. Пробл. стандартизации в здравоохр. 2005; 3: 74–166.
- Chwieduk C.M., Curran M.P. Pramipexole extended release in Parkinson’s disease. CNS Drugs 2010; 24: 327–336.
- Grosset K.A., Bone , Grosset D.G. Suboptimal medication adherence in Parkinson’s disease. Mov. Disord. 2005; 20: 1502–1507.
- Hauser R., Salin L., Koester J. Double-blind evaluation of pramipexole extended-release (ER) in early Parkinson’s disease. Neurology 2009; 72 (11 Suppl. 3): A412–413.
- Kvernmo T., Härtter S., Bürger E. A review of the receptor-binding and pharmacokinetic properties of dopamine agonists. Clin. Therap. 2006; 28: 1065–1078.
- Mizuno Y., Yamamoto M., Kuno S. et al. Efficacy of Pramipexole Extended Release (ER) and switching from Pramipexole Immediate Release (IR) to ER in Japanese advanced Parkinson’s disease (PD) patients. In: XVIII WFN World Congress on Parkinson’s Disease and Related Disorders: Miami Beach, 2009: Poster 2.192.
- Möller J.C., Oertel W.H. Pramipexole in the treatment of Parkinson’s disease: new developments. Expert Rev. Neurother. 2005; 5: 581–586.
- Poewe W., Rascol O., Barone P. et al. Pramipexole extended-release in early Parkinson’s disease. Neurology 2011; 77: 759–766.