Внимание!
Информация в статье является справочной и не может использоваться для самодиагностики и самолечения. Для расшифровки результатов анализов обратитесь к специалисту.
Раньше это состояние считали обычными возрастными изменениями, сопутствующими старению организма. Сейчас стараются его выявить у больных как можно раньше, чтобы замедлить процесс деградации нейронов при помощи лекарств.
Болезнь Альцгеймера — что это?
Болезнь Альцгеймера – это прогрессирующая форма сенильной деменции, приводящая к исчезновению когнитивных способностей. Его относят к группе приобретенных нейродегенеративных патологий. Заболевание возникает чаще у пациентов в возрасте старше 65 лет. Реже отмечают формы, начинающиеся ранее 60 лет. Болезнь развивается постепенно и незаметно.
У больного сначала появляются расстройства кратковременной памяти и внимания. Затем симптомы неуклонно нарастают. У человека грубо нарушаются внимание, память, речь. Пациент не может вырабатывать новые навыки и воспроизводить старые. У него нарушается психомоторная координация, страдает ориентация во времени.
Пациент дезориентирован в пространстве, месте и собственной личности. Выявляют расстройство мышления. Все патологические процессы обусловлены разрушением клеток головного мозга. Различают два типа течения болезни Альцгеймера. Первый — раннее начало заболевания с дебютом клинических проявлений после 65 лет, второй тип с началом симптомов до 65 лет.
Диагноз устанавливают, основываясь на клинической картине после исключения заболеваний со сходной клиникой. Выставленный диагноз подтверждается посмертно при проведении аутопсии. Определяется число нейрофибриллярных сплетений и сенильных бляшек.
Роль диеты в развитии болезни Альцгеймера
15.12.2020 1859
Регулярное употребление некоторых продуктов, в том числе сыра и красного вина, может замедлить снижение когнитивных функций и препятствовать развитию таких нейродегенеративных заболеваний, как болезнь Альцгеймера. К такому выводу пришли на основании широкомасштабного исследования ученые из Университета штата Айова (США). Результаты работы исследователей опубликованы в последнем выпуске американского медицинского журнала Journal of Alzheimer»s Diesease.
Режим питания, пища, которую употребляет человек на протяжении жизни и, особенно, в пожилом возрасте сказывается не только на его поведении в целом, но и существенным образом влияет на его когнитивные способности, отмечается в исследовании. «Наша работа является по сути первой, в которой поднимаются вопросы связи диеты и познавательных процессов, особенно в пожилом возрасте», — говорит руководитель проекта, доцент Университета штата Айова Ауриэль Виллет (Auriel Willette). По его словам, проследить образ жизни и состояние здоровья 1 787 людей в возрасте от 46 до 77 лет помогла обширная база данных, предоставленная британским Biobank, в котором содержатся разнообразные сведения о более чем полумиллионе пациентов, в том числе генетические данные, результаты клинических анализов, функциональных исследований. С целью выявления степени сохранности когнитивных функций респондентам был предложен тест — Fluid Intelligence Test (FIT). Исходный уровень когнитивных способностей был составлен на основании результатов опросов в течение 2006–2010 годов, следующие фазы исследований распределились между 2013-2015 и 2015–2016 годами. Помимо этого, пациенты ответили на вопросы о своих пищевых предпочтениях, употреблении алкоголя, особенно вина, пива и крепких напитков. Результаты исследования показали, что сыр и красное вино — именно те продукты, употребление которых защищает мозг человека от когнитивных «провалов» даже в позднем возрасте. Как утверждают ученые, поддержанию на должном уровне познавательных функций пожилых способствует и еженедельное употребление баранины. Исследователям не до конца удалось прояснить роль в рационе излишков соли, но все же они рекомендовали людям с предрасположенностью к нейродегенеративным заболеваниям ограничить ее прием. «Наша работа явно свидетельствует о роли сыра и красного вина в профилактике интеллектуальных потерь пожилого поколения, — делится результатами исследования Виллет. — В разгар пандемии коронавируса данный рацион позволяет поддерживать организм в тонусе даже в позднем возрасте. Это очень важно, поскольку всем известно, насколько тяжело организовать уход за пациентами с деменцией в условиях самоизоляции и дистанцирования». Соавтор исследования, доктор философии, невролог Университета штата Айова Брэндон Клайндинст (Brandon Klinedinst) убежден, что «коррекция питания — один из механизмов регулирования информационной системы человека на генном уровне, позволяющих помочь человеку сохранить интеллект в любом возрасте». Источник: Информационное агентство ТАСС https://content.iospress.com/search?q=Klinedinst&published_between=&from_year=&to_year=
Поделитесь новостью в социальных сетях
Предыдущая новость Следующая новость
16.12.2020
Причиной возникновения шизофрении может быть дефект иммунной системы челове…
1139
13.12.2020
Опубликован закон о реформе системы ОМС
1675
Все новости
Стадии
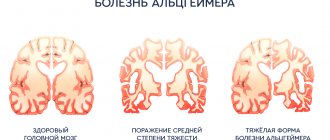
Течение болезни делят на четыре фазы, с прогрессирующей клинической картиной с когнитивными и функциональными нарушениями. Выделяют следующие стадии:
- Предеменция. Первые проявления болезни Альцгеймера часто схожи с реакцией на стресс или обычными возрастными изменениями. Изменения когнитивных функций обнаруживают за восемь лет до развернутой стадии при нейрокогнитивном тестировании. Начинаются проблемы с неспособности усвоения новой информации. Больные не могут сосредоточиться. Страдает планирование, отсутствует когнитивная гибкость. Нарушается абстрактное мышление, снижается семантическая память.
- Ранняя деменция. Прогрессирует ухудшение памяти, нарушение всех видов восприятия при болезни Альцгеймера ведут к подтверждению диагноза. Память снижается неравномерно. Старые воспоминания о своей жизни и давно выученные факты сохраняются. Быстро забываются недавно выученные факты. Появляются речевые нарушения. Возникают дефекты исполнительных функций, двигательные нарушения, расстройства восприятия. Происходит оскудение словарного запаса, снижается беглость речи. Появляется неловкость при использовании тонкой моторики, нарастают проблемы с координацией. Человек способен выполнять независимо только простые задачи.
- Умеренная деменция. У больных происходит прогрессирующее ухудшение состояния. Снижается возможность независимых действий. Становятся очевидными расстройства речи, резко обеднен словарный запас. Человек неверно подирает по смыслу слова. Теряются навыки чтения и письма. Нарушается координация при сложных последовательных движениях. Человек не справляется с большинством обычных задач. Больной не узнает близких родственников. Ухудшается долговременная память. Появляются нейропсихиатрические изменения – раздражительность, бродяжничество, эмоциональная лабильность, спонтанная агрессия.
- Тяжёлая деменция. На этой стадии болезни пациент зависим от посторонней помощи. Он при общении использует единичные фразы и слова. Затем речь полностью исчезает. Сохраняется реакция на эмоциональное обращение к ним. Иногда возникают эпизоды агрессии, которые сменяются апатией и истощением. Даже самые простые действия невозможны без посторонней помощи. У пациента снижается мышечная масса. Он передвигается с трудом, часто не в силах встать с кровати.
Смерть наступает от сопутствующих причин — пролежневых язв, пневмонии и других заболеваний.
Как организовать эффективное питание при болезни Альцгеймер?
Пациенты с неврологическими заболеваниями и их близкие подвергаются целому ряду испытаний. Большая часть из них связана с питанием. Диагнозы неврологического толка чаще всего сопровождаются проблемами с жеванием, глотанием и перевариванием пищи. Из-за этого больные не могут полноценно питаться, теряют вес, их организм истощается и становится подвержен различным инфекциям. В результате поражения головного мозга пациенты часто испытывают трудности с координацией движений и обслуживанием себя, что тоже затрудняет приготовление и приём пищи. Хроническая недостаточность кровоснабжения головного мозга, гибель нейроновприводят к развитию у больного деменции. В этих случаях врачи зачастую советуют рассмотреть вариант нутритивной поддержки. Энтеральное питание помогает бороться с истощением или предотвратить его, облегчает процесс приёма пищи и упрощает уход за больным человеком. Своевременно подобранное питание даст возможность скорректировать симптомы заболевания и улучшить общее состояние больного. Врач поможет правильно подобрать лечебное питание и рассчитать его количество в соответствии с индивидуальными потребностями в энергии и белке с учётом диагноза, возраста и общего состояния организма.
Проблемы, связанные с питанием, пациентов с болезнью Альцгеймера:
- Риск снижения веса. Люди с болезнью Альцгеймера страдают нарушением памяти: они могут забыть поесть, не заметить, что голодны или вовсе не узнать еду. Также из-за небольшой физической нагрузки у них может отсутствовать аппетит, а лекарства могут изменять обоняние и вкус. Из-за этого пациенты мало едят, иногда совсем отказываются от еды, а в результате могут сильно похудеть, их организм может быть так ослаблен, что увеличивается риск падений, травм и различных заболеваний. В этих случаях рекомендуется богатая белком пища и достаточное количество жидкости.
- Большой аппетит, отсутствие чувства насыщения. Некоторые пациенты с болезнью Альцгеймера, наоборот, едят очень много сладостей. В таком случае важно контролировать пациента и стараться, чтобы рацион был разнообразным и полноценным. Но делать это следует аккуратно: резкая смена меню и ограничения могут вызвать у больного стресс.
- Сложности с самообслуживанием. На определённых стадиях болезни Альцгеймера пациентам сложно есть самостоятельно: тяжело держать ложку или положить необходимое количество еды в тарелку и т.д. В этом случае нужно мягко напоминать больному о необходимости поесть, лучше устраивать совместные трапезы. Важно, заранее подготовить пищу и напитки нужной температуры и консистенции.
- Запоры, тошнота, вздутие живота.Эта проблема очень распространена среди пациентов с болезнью Альцгеймера. В этом случае может помочь увеличение физической активности, включение в меню продуктов, богатых клетчаткой, и потребление большого количества жидкости.
Рекомендации по организации питания пациентов с болезнью Альцгеймера:
- Следует напоминать больному о необходимости приёма пищи.
- Садитьсяза стол лучше в спокойной обстановке, чтобы пациента не отвлекали посторонние шумы (тв, радио и т.п.)
- Не нужно торопить больного, наоборот следует попросить его не спешить и успокоить, если что-то не получается.
- Пациент должен быть в нормальном настроении, он не должен быть возбуждён или подавлен. Не стоит кормить его насильно.
- Напитки и еда должны быть нормальной температуры. Их заранее стоит остудить или подогреть: у больного может пропасть ощущение холодного и горячего.
- Лучше подавать еду, которую можно есть руками, т.к. на определённых стадиях деменции пациент не может пользоваться столовыми приборами или может нанести себе травму.
- На поздних стадиях деменции еда должна быть в жидком виде или в виде пюре.
- Говорите названия блюд и напитков, которые подаёте. Так больной сможет дольше удерживать их в памяти, и это облегчит ваше общение.
- Важно отслеживать рацион: пациент должен получать нужное количество питательных веществ.
Вместо заключения:
Питание напрямую влияет на развитие болезни Альцгеймера. Правильный рацион пожилых людей может улучшить когнитивные функции, замедлить развитие и облегчить течение деменции. Когда диагноз поставлен, следует совместно с лечащим врачом составить план нутритивной поддержки, чтобы пациент получал необходимое количество питательных веществ, а уровень его жизни оставалсядостаточно высоким. Поделиться:
(3 оценок; рейтинг статьи 2.7)
Причины
Единственного фактора, ответственного за возникновение болезни Альцгеймера не выявлено. Считают, что к заболеванию существует наследственная предрасположенность. Сейчас вдвигают несколько гипотез формирования изменений в головном мозге:
- Холинергическая. Когнитивный дефицит связан с замедлением образования нейромедиатора ацетилхолина. Теория считается устаревшей, но от нее полностью не отказываются.
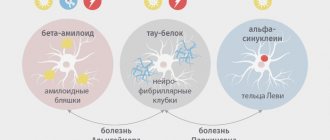
- Амилоидная. Основным фактором развития изменений в мозге при болезни Альцгеймера считают отложение в его тканях бета-амилоидного белка. Дефект митохондриальной ДНК находят у половины больных. Ген, кодирующий его образование, находится в 21 хромосоме. Раннее начало болезни связывают с дефектами генов PSEN1, АРР, PSEN2. Появляются бляшки бета-амилоида в мозге, замедляющие скорость когнитивных реакций. Данная гипотеза признается основной. Накопление амилоида запускает цепь нейродегенеративных расстройств.
- Тау-гипотеза. Считают, что каскад патологических изменений инициирует отклонение структуры тау-белка. В нем гиперфосфорилированные нити соединены. В нейронах идет формирование нейрофибриллярных клубков. Затем происходит дезинтеграция микротрубочек. Разрушается транспортная система в клетках. Это нарушает между нейронами систему передачи сигналов.
- Инфекционная. Полагают, что развитие болезни связано с возбудителем периодонтита. Происходит колонизация тканей мозга бактериями, что увеличивает выработку бета-амилоида.
Исследователи отмечают, что высокое потребление сахара ускоряет развитие когнитивных нарушений. Это ухудшает течение заболевания.
PsyAndNeuro.ru
На данный момент ВОЗ при лечении болезни Альцгеймера рекомендует при легкой и умеренной степени деменции назначать ингибиторы холинэстеразы, а при умеренной и тяжелой – мемантин. Также, в этом году был одобрен адуканумаб, но его место в лечении патологии пока не определено в полной мере.
Результаты клинических испытаний, на основе которых принимаются решения о разработке новых лекарств, обычно представлены в виде сравнения количественных различий между группами по соответствующим шкалам симптомов. Для интерпретации результатов клинических испытаний, принятия клинических решений и разработки исследований с достаточной статистической мощностью необходимо решить, какой эффект лечения можно считать Минимальным клинически значимым изменением (MCID – minimum clinically important difference). В отношении исследований Болезни Альцгеймера (БА) единого мнения о MCID не существует. Несмотря на то, что Управление по контролю за продуктами и лекарствами США (FDA) в 1989 г. составило руководство по одобрению новых антидементных препаратов, до сих пор нет точного определения MCID.
Консультативный комитет FDA по периферической и центральной нервной системе 6 ноября 2021 г. почти единогласно проголосовал против одобрения адуканумаба. Однако его рекомендация была отвергнута и FDA в итоге одобрило использование этого препарата для лечения БА. Ситуация с адуканумабом заставляет вновь обратится к вопросу: как определить эффективность антидементного лечения?
В 1989 г. тот же Консультативный комитет FDA решил, что разница в 3 балла по шкале оценки симптомов БА ADAS-Cog – это признак клинически значимого изменения в состоянии пациента. Однако наличие статистически значимой разницы может объясняться случайностью. Любой эффект, превышающий нулевой эффект, может быть статистически значимым при достаточно большом размере выборки. Таким образом, по-прежнему не найден консенсус по вопросу MCID в исследованиях лечения БА.
FDA признает лечение легкой и умеренной стадии деменции при БА эффективным, если есть положительная динамика в основной симптоматике (когнитивные функции) и глобальной клинической картине (по оценке лечащего врача) или в функциональности (активность пациента в повседневной жизни). Для исследований, включающих продромальных пациентов с легкими когнитивными нарушениями, FDA требует доказать только статистически значимые изменения заранее определенных параметров, включающих в себя когнитивные и повседневные функции. В 2013 г. FDA рекомендовало использовать для этого комплексный инструмент оценки Clinical Dementia Rating Sum of Boxes (CDR-SB). Статистически значимое улучшение CDR-SB показывает тогда, когда фиксируются изменения основной симптоматики (память, ориентация, решение задач, логическое мышление) и одновременно улучшается функциональность (быт, повседневные дела, хобби). У Европейского Медицинского Агентства похожий подход. Тем не менее, остается вопрос – не слишком ли низко установлена планка для определения эффективности?
Исследование, проведенное в 2021 году, показало, что MCID увеличивается вместе со степенью тяжести заболевания. Для легкого когнитивного расстройства и БА легкой степени MCID составляет соответственно 0,98 и 1,63 балла по шкале CDR-SB, 1,26 и 2,32 балла по шкале MMSE. В исследовании 2012 г. сообщалось, что MCID у пациентов с легкой степенью БА составляет 3 балла по шкале ADAS-Cog11.
Однако эти значения MCID не являются обязательным условием для получения одобрения FDA. Примечательно, что в ходе испытаний адуканумаба пороговые значения MCID ни по шкале CDR-SB, ни по шкале MMSE достигнуты не были (CDR-SB -0,39; MMSE 0,6).
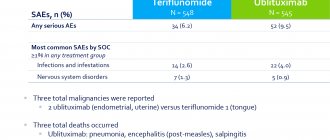
Мемантин и другие одобренные антидементные препараты безопасны и хорошо переносятся, в то время как высокие дозы адуканумаба ассоциированы с 35-процентной вероятностью отека мозга, 20-процентной вероятностью микрокровоизлияний в мозге (в плацебо-группе соответственно 2 % и 7 %). Побочные действия повышают риск того, что нарушится условие ослепления в экспериментальной группе, принимающей высокие дозы адуканумаба, и, как следствие, искажается результат оценки по опросникам, которые заполняются с участием ухаживающих лиц.
Незначительный эффект адуканумаба сравним с эффектом, который показали другие препараты, воздействующие на амилоид. Вероятно, уменьшение амилоида само по себе не приводит к клинически значимому улучшению когнитивных функций, тогда как применение мемантина достоверно положительно влияет на эти показатели. Мета-анализ 2021 г. показал, что снижение уровня амилоида на 0,1 единицы стандартизованного уровня захвата при приеме адуканумаба приводит к улучшению по шкале MMSE на 0,03 балла, в то время как прием препарата Меманталь* за 3 месяца терапии показывает повышение данного показателя на 2 балла.
Установленная регуляторами низкая планка оценки эффективности побуждает спонсоров исследований увеличивать размер выборки для того, чтобы с большей вероятностью найти статистически значимое изменение. Например, 78-недельное исследование адуканумаба планировалось проводить с 1350 участниками, но их количество было увеличено до 1647 в тот момент, когда стало ясно, что статистически значимое изменение может быть не обнаружено.
Клинические исследования когнитивных нарушений должны быть организованы так, чтобы их результаты отражали значимые изменения. Руководства для проведения испытаний новых препаратов от БА должны включать определения клинически значимых изменений, по крайней мере, по шкалам CDR-SB и MMSE. Использование четко определенного MCID придаст ясность и укрепит уверенность в результатах испытаний, что принесет существенную пользу пациентам и системе здравоохранения в целом.
*Меманталь – мемантин производимый на территории ЕС компанией Синтон, Испания. Поставляется в Россию, Великобританию, Голландию, Францию, Германию и др. страны.
Автор: Филиппов Д.С.
Источник: Liu K., Schneider L., Howard R. The need to show minimum clinically important differences in Alzheimer’s disease trials // Lancet Psychiatry, Published Online June 1, 2021
Симптомы
Начальные признаки изменений практически заметны. Проявления болезни развиваются постепенно и медленно, они следующие:
- у больного возникают трудности с памятью на недавние события;
- присутствуют эмоциональные расстройства;
- плохая узнаваемость известных предметов;
- нарушаются высшие корковые функции;
- снижение возможности ориентирования в пространстве;
- депрессия;
- безразличие;
- беспокойство.
В дальнейшем у больного нарастают когнитивные расстройства. Он неспособен принимать решения. С трудом не выполнятся математические операции, что затрудняет подсчет денег. Речь становится бессвязной. Появляются длительные паузы, которые связаны с долгим подбором слов. Для поздней стадии болезни характерна следующая клиника:
- бред;
- неузнавание близких людей;
- галлюцинации;
- судороги;
- шаркающая походка;
- утрата способностей к самостоятельному передвижению;
- деградация личности;
- нарушение ориентации в месте и времени;
- отсутствие возможностей мыслительной деятельности.
При тяжелой деменции пациент полностью зависит от посторонних. Он не может обслужить себя. Пропадают приобретенные навыки, теряется членораздельная речь. Агрессия чередуется с апатией и истощением.
Диагностика
При подозрении на заболевание пациенты обращаются к психотерапевту или неврологу. Врач осматривает больного, изучает его анамнез. Беседует с больным и его родственниками. Основным критерием для постановки диагноза считают наличие снижения памяти и познавательных способностей. Назначают дополнительные методы исследования:
- КТ и МРТ головного мозга;
- анализ спинномозговой жидкости на бетта-амилоидный белок;
- тест «NuroPro»;
- генетическое тестирование;
- определение уровня в крови бета-амилоида;
- позитронно-эмиссионная томография.
Пациенту проводят тесты на определение когнитивных способностей – цифровые, Sage-тест, изображение часов.
Лечение
До настоящего времени лечения способного прекратить развитие болезни Альцгеймера не найдено. Существуют лекарственные средства, замедляющие прогрессирование симптоматики. К ним относят следующие препараты:
- NMDA-антагонисты;
- ингибиторы холинэстеразы;
- ингибитор бета-секретазы.
Для облегчения симптомов назначают нейролептики и лекарства, усиливающие мозговое кровообращение. Назначается низкокалорийная диета, обогащенная белком. Рекомендуют снизить количество сахара и соли. Нужно есть жирную рыбу, продукты с высоким содержанием витаминов группы В, селена, цинка.
Важное место в улучшении самочувствия пациента играет психотерапевтическая поддержка. Больному важно отсутствие стрессовых ситуаций, пребывание в комфортных условиях. Необходимо ему создавать положительный эмоциональный настрой.
Препараты второй линии при лечении болезни Альцгеймера
Самые эффективные препараты при болезни Альцгеймера – это ингибиторы холинэстеразы. Однако, лечение патологии должно быть комплексным с устранением клинических проявлений.
Какими лекарствами лечат болезнь Альцгеймера:
- Для улучшения мозгового кровообращения и нормализации эмоционального фона может быть использован Глицин;
- Для устранения галлюцинаций и появления навязчивых идей могут применяться нейролептики и транквилизаторы;
- Лечение чувства тревожности, панических атак, депрессивного состояния выполняется с помощью антидепрессантов.
Все препараты для терапии болезни Альцгеймера должны назначаться лечащим врачом неврологом. Каждый из препаратов имеет свои противопоказания и побочные эффекты, поэтому самостоятельное их применение может негативно отразиться на состоянии здоровья.
Дополнительно к медикаментозному лечению пациенту назначают и другие виды терапии:
- Лечебная гимнастика;
- Аква-аэробика;
- Арт-терапия;
- Специальные занятия для улучшения когнитивных функций.