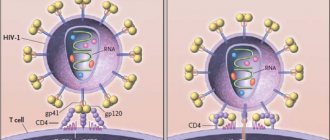
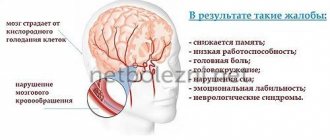
Перинатальная энцефалопатия новорожденных – неклассифицируемое невоспалительное нарушение нервной системы, наблюдающееся во время беременности или сразу после появления на свет.
Неклассифицируемым заболевание называют потому, что энцефалопатия не определяется традиционными анализами. Даже высокотехнологичные исследования не дают полной объективной картины.
Понятие перинатальной энцефалопатии (ПЭ) исключено из Международной классификации. Сегодня энцефалопатию определяют как последствия поражения головного мозга плода. Если придерживаться точности терминологии, то энцефалопатию можно назвать следствием деструктивных проявлений, разрушающих кору мозга.
Причины перинатальной энцефалопатии.
Признаки патологии часто неконкретны. Для выявления проблемы иногда требуются динамическое наблюдение на протяжении длительного времени. Есть сведения, что на первичном приеме невролога до 80% детей получает диагноз ППЭ или «перинатальная энцефалопатия неуточненная». Успокаивает тот факт, что к году у большинства детей диагноз снимают. Объяснить это можно отсутствием четких критериев диагностики и мобильностью нейропсихологического строя младенца. Перинатальная энцефалопатия – органические и функциональные нарушения головного мозга у детей в дни внутриутробного развития и первые часы жизни. Временные границы определяются такие: с 28-й недели беременности до 7-го дня после рождения. У недоношенных детей срок продлевается до 28 суток.
Серьезность недуга и сложность диагностики не являются приговором. Основные факторы, служащие причинами болезни, все же существуют:
- Гипоксия – нехватка кислорода, имеет ишемическую природу. При прекращении поступления кислорода кровь перестает поставлять питание и наполняется углекислым газом. Это соединение провоцирует окисление клеток. В результате, появляется ацидоз (синдром «окисления организма») – расстройство кислотно-щелочного баланса. Самое опасное его последствие — отек.
Гипоксия может оказывать как разрушающее, так и восстанавливающее действие. Сразу после выхода ребенка из утробы ацидоз выступает в качестве средства адаптации при перемене среды его обитания. При затяжной его форме проявляется энцефалопатия новорожденных.
При осложненном рождении наступает асфиксия – кислородное голодание головного мозга детей. Тогда может случиться некомпенсированный ацидоз. В результате нарушения кровоснабжения головного мозга меняется кислотно-щелочной баланс (он измеряется показателем pH). При некомпенсированном ацидозе малыша показатель падает ниже 7,1, что требует немедленных реанимационных мер.
- Черепная травма. Она влечет за собой посттравматическую энцефалопатию. В результате тяжелых родов у ребенка наблюдаются психические и физические расстройства. В зависимости от степени тяжести травмы энцефалопатия новорожденных может выражаться в разных формах.
- Поражение лобных или височных долей головного мозга в момент родов;
- Отек головного мозга, нарушение кровоснабжения клеток соединительным материалом: при этом возникают спайки и рубцы;
- Аутонейросенсибилизация – конфликт иммунной системы: она ошибочно начинает реагировать на собственные клетки как на инородный объект.
- Токсико-метаболический синдром — результат токсического воздействия метаболической деятельности нездоровых почек, желчевыводящих путей у детей. Довольно широко распространена билирубиновая энцефалопатия (желтуха новорожденных), т. е. интоксикация билирубином. Билирубин является нейротоксическим ядом, приводящим к повреждению коры головного мозга и подкорковых ядер. В зависимости от причин различают несколько видов желтухи новорожденных: коньюгационная (низкая связывающая способность печени), гемолитическая (вызванная гемолизом – разрушением эритроцитов), обтурационная (проблемы с оттоком желчи), паренхиматозная.
- Внутриутробные инфекции заражают новорожденного, провоцируют воспалительные процессы. Инфицирование плода может привести к серьезной патологии нервной системы, перинатальной энцефалопатии, преждевременным родам и даже к гибели ребенка.
- Нарушение маточно-плацентарного кровотока (фетоплацентарная недостаточность) – сбой кровообращения в плаценте в позднем периоде вынашивания. Через эту защитную оболочку происходит питание плода, обеспечение его кислородом, осуществляется гормональный обмен. Когда дисфункция незначительна — опасность минимальна, но при серьезной фетоплацентарной недостаточности наступает гипоксия с последующей энцефалопатией.
- Тяжелая хроническая или острая болезнь матери также негативно влияет на ребенка. Гестоз – осложнение позднего периода беременности, его именуют поздним токсикозом. Вследствие заболевания происходит поражение внутренних структур матери (почки, печень, кровообращение).
- Угроза прерывания беременности таит в себе множество негативных побочных эффектов, включая вышеназванные факторы.
Причины возникновения
Гипоксическая энцефалопатия у взрослых и у детей возникает по разным причинам. Их важно знать, чтобы принять все меры для ее предупреждения.
У взрослых
Гипоксическая ишемическая энцефалопатия возникает на фоне нехватки кислорода, к чему приводят следующие причины:
- состояние удушья;
- удушение;
- сбой дыхательной системы любого рода происхождения;
- наркотическая зависимость, передозировка;
- патологии кровеносной системы, приводящие к ее непроходимости или разрыву;
- цианид, окись углерода — отравление;
- длительное пребывание в задымленном месте;
- травма трахеи;
- остановка сердца;
- болезни, приводящие к параличу мышечной ткани дыхательной системы.
Острая гипоксическая энцефалопатия наступает, если кислород не поступал в организм несколько минут. Это тяжелое течение патологии, которое чаще всего заканчивается летальным исходом. Зафиксированы единичные случаи, когда люди выживали, но для них это заканчивалось тяжелой формой серьезных психических болезней.
У новорожденных
Причиной такого состояния у только родившегося ребенка может быть:
- удушье во время родов из-за слабой родовой деятельности;
- преждевременный родовой процесс или с патологическими факторами, такими как выпадение пуповины;
- болезни инфекционного генеза у матери;
- ряд физических факторов от грязного воздуха до радиационного излучения.
Именно асфиксия у грудничков является самым частым фактором, приводящим к ГИЭ. Врачи выделяют следующие факторы риска для ее возникновения:
- гипотония острой формы у роженицы;
- недоразвитость легких, что приводит к недостатку кислорода в крови;
- сложности в работе сердца;
- травмирование плода узким тазом матери или из-за проблем с пуповиной;
- сложности в родовой деятельности, травма, стресс;
- гипоксия;
- родовое кровотечение;
- халатность медицинского персонала;
- отслойка плаценты;
- изменение формы черепа плода из-за давления;
- родовая травма, разрыв матки;
- низкое предлежание плаценты.
РЕКОМЕНДУЕМ ПОСМОТРЕТЬ: Причины кистозно атрофических изменений головного мозга
Диагностика энцефалопатии.
Симптомы у детей проявляются не сразу. Немедленное установление уровня и характера проблемы в первые дни после рождения может представлять сложность.
Иногда за симптомы энцефалопатии принимают естественные проявления нервной организации новорожденного, в других случаях — заболевание остается незамеченным. Объективные выводы зачастую можно сделать только спустя полгода. По правилам, осмотр ребенка врачом производится каждый месяц в первом полугодии его жизни. Врач исследует рефлексы малыша, определяет качество его физического развития. В достаточно короткий отрезок времени возможно не только диагностировать аномалию, но и успешно исправить ее. Может потребоваться длительное динамическое наблюдение для того, чтобы диагноз не порождал сомнений, и выработка схемы лечения болезни стала возможной.
Глубина поражения мозга ребенка бывает разная. В зависимости от тяжести заболевания установлены 3 уровня мозговых деструкций, имеющих отдаленные последствия:
- Начальная степень заболевания характеризуется небольшим замедлением моторного развития детей более чем на 2 недели. При первой степени, к счастью, не страдают вещества головного мозга.
- Отклонения средней тяжести определяются наличием судорог при плаче, отставанием малыша в моторике на 8 недель, при гипервозбудимости, синюшности при непродолжительном плаче, «мраморности» кожи, подергивании рук и ног. Развивается мышечный гипертонус, выявляется адаптационные синдромы. Через год заболевание «предлагает» новые симптомы (пытаясь ходить, ребенок опирается на носок). Отсутствие лечения в дальнейшем грозит серьезными отклонениями.
- Глубокое повреждение головного мозга выражается в церебральном параличе (ДЦП) и аутизме. К помощи восстановительной медицины следует прибегнуть на как можно более раннем периоде.
Причины и стадии гипоксически-ишемического поражения
Перинатальное поражение ЦНС у новорожденных формируется при действии неблагоприятных факторов внутриутробно, в родах либо во время новорожденности. Причинами этих изменений способны стать:
- Расстройства кровотока в матке и плаценте, кровотечения у беременных, патология плаценты (тромбозы), отставание развития плода;
- Курение, употребление алкоголя, прием некоторых лекарственных препаратов во время беременности;
- Массивные кровотечения во время родов, обвитие пуповины вокруг шеи плода, выраженная брадикардия и гипотония у младенца, родовые травмы;
- После родов — гипотония у новорожденного, врожденные пороки сердца, ДВС-синдром, эпизоды остановки дыхания, нарушения функции легких.
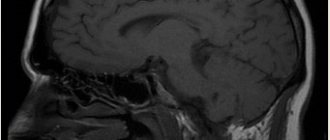
пример гипоксически-ишемического поражения мозга
Начальным моментом развития ГИЭ служит дефицит кислорода в артериальной крови, который провоцирует патологию метаболизма в нервной ткани, гибель отдельных нейронов или целых их групп. Головной мозг становится чрезвычайно чувствительным к колебаниям артериального давления, а гипотония только усугубляет имеющиеся поражения.
На фоне метаболических нарушений происходит «закисление» ткани (ацидоз), нарастает отек и набухание мозга, увеличивается внутричерепное давление. Эти процессы провоцируют распространенный некроз нейронов.
Тяжелая асфиксия отражается и на работе других внутренних органов. Так, системная гипоксия вызывает острую почечную недостаточность из-за некроза эпителия канальцев, некротические изменения слизистой кишечника, поражения печени.
У доношенных детей отмечают постгипоксическое поражение преимущественно в области коры, подкорковых структур, ствола мозга, у недоношенных ввиду особенностей созревания нервной ткани и сосудистого компонента диагностируется перивентрикулярная лейкомаляция, когда некрозы сконцентрированы преимущественно вокруг боковых желудочков мозга.
В зависимости от глубины ишемии мозга выделяют несколько степеней тяжести гипоксической энцефалопатии:
- Первая степень — легкая — преходящие нарушения неврологического статуса, продолжающиеся не более недели.
- ГИЭ второй степени — длится дольше 7 суток и проявляется угнетением либо возбуждением центральной нервной системы, судорожным синдромом, временным увеличением внутричерепного давления, вегетативной дисфункцией.
- Тяжелая форма гипоксически-ишемического поражения — расстройство сознания (сопор, кома), судороги, проявления отека мозга со стволовой симптоматикой и нарушением деятельности жизненно важных органов.
Что должно насторожить родителей.
Особенность энцефалопатии заключается в необходимости максимально раннего начала стабилизации и устранения неврологических дефектов плода.
Формирующиеся синдромы можно остановить и исправить на протяжении беременности и во младенчестве, но требуется квалифицированная помощь невролога.
Особая ответственность возлагается на родителей. Вызвать беспокойство должна одна из особенностей поведения или самочувствия ребенка:
- нарушения сна;
- гипертонус мышц;
- плохая координация;
- вялость рук;
- не переворачивается;
- ноги не участвуют в ползании;
- не садится и не встает;
- неправильное ползание;
- повышенная возбудимость при разных раздражителях (часто плачет);
- угнетенный вид в фазе бодрствования;
- синдром отставания моторного развития (не берет в руку игрушку);
- может подтягиваться только на правой руке;
- срыгивание фонтаном после еды;
- тремор – мелкое дрожание мышц;
- масса тела медленно увеличивается;
Такие симптомы заставляют обратиться в клинику. Нельзя пренебрегать важными профилактическими мерами, даже если кажется, что ребенок здоров.
Что важно предпринять вовремя:
- Тщательный осмотр неврологом в возрасте ребенка 4 недели.
- Регулярный ежемесячный осмотр педиатром, а если понадобится — лечение заболевания.
- Сделать тест нейросонографии — НСГ (устанавливает синдром двигательного нарушения).
Если уже установлено наличие ДЦП или эпилепсии, необходимо как можно быстрее начинать лечение для предотвращения дальнейшей патологии.
Остеопатия в коррекции энцефалопатии новорожденных.
Органические нарушения развития головного мозга у младенцев необходимо выявлять и лечить немедленно.
Из-за нейронных нарушений возникают заболевания внутренних органов ребенка. Поврежденная сеть начинает управлять всем организмом. Происходит также и обратное влияние: нормализация почек, печени, легких воздействует на нейронные связи. Поэтому при стабилизации мозга необходимо учитывать общую картину развития организма, искать варианты комплексного лечения.
Остеотерапия – одна из ветвей восстановительной медицины. Человек рассматривается как единая целостная схема. Основные принципы методики провозглашены более 30 лет назад. За несколько десятилетий выработаны новые подходы, найдены способы управления, приобретен практический опыт. Медикаментозные препараты используются с большой осторожностью или отсутствуют вообще. Лечение происходит с помощью мобилизации всех элементов, включенных в восстановление. Преимущества данной области медицины в том, что препараты практически не применяются. Ребенок активизирует свои внутренние резервы. Комплексное лечение – основа теории.
Определились следующие остеопатические направления:
краниосакральный
структуральный
висцеральный
фасциальный
1. Краниосакральный метод лечения.
Краниосакральный (cranium-череп, sacrum-крестец) путь основан на теории, согласно которой кости черепа подвижны (раньше считалось, что подвижна только нижняя челюсть). Динамика их движения незаметна и строго подчиняется импульсам мозга. Если организм в целом и главный центр управления функционируют нормально, то ритм движения элементов черепа четкий и правильный. Сбой мозговых импульсов на фоне энцефалопатии свидетельствует об отклонениях от нормы. Изучение ритмики движения черепных участков детей используется не только для диагностики и выявления нервной деструкции, но и для обратного процесса. Через систематизацию импульсов возможно воздействие на поврежденную зону. Особенно эффективен данный способ в устранении последствий энцефалопатии.
Лечение участков мозга устраняет симптомы болезни, нормализует внутричерепное давление детей и может привести к восстановлению пораженных участков.
2. Структуральный метод.
Объектом структурального воздействия выбран опорно-двигательный аппарат новорожденного.
Костная и хрящевая субстанции оказывают влияние на функцию спинного мозга. Нейронные волокна, вены, связанные с позвоночником, также встроены в общую схему. Лечение конечностей, шеи, хребта способствует нормализации отдельных поврежденных зон головного мозга, пострадавших вследствие патологии (перинатальная энцефалопатия).
Структуральная теория в энцефалопатии оперирует мерами воздействием на кости и для избавления от проблем формирования плода и их влияния применяется нечасто.
3. Фасциальный метод.
Фасциальная терапия исследует мягкие ткани, слизистые оболочки, кровопроводящие пути. Лечение энцефалопатии основано на вырабатывании нейронных связей между отдельными участками тела. Фасциальный способ устраняет вегетативно-висцеральные расстройства мозга детей и их следствие — гипервозбудимость. Лечение энцефалопатии фасциальными приемами заключается в коррекции мышечной дистонии, если есть признаки повышенного тонуса мышц.
4. Висцеральный метод при коррекции энцефалопатии.
Висцеральная терапия использует способность внутренних структур к взаимодействию и взаимовлиянию. Так, билирубиновая энцефалопатия требует синхронизации работы печени.
Синдром церебральной ишемии, связанный с гипоксией, проявляется в неправильной деятельности сердца и легких. Лечение осуществляется комплексное (препараты используются минимально).
Дальнейшее наблюдение
Из стационара выписывают только после прохождения полного курса физической терапии и комплексной оценки нервно-психического развития. Чаще всего после выписки пациенты не требуют специфического ухода, но регулярные осмотры в клинике обязательны, особенно для детей.
Если болезнь была тяжелой, то ребенок будет наблюдаться в специальном центре, где ему будет помогать врач по нервно-психическому развитию.
Лечение судорожности зависит от симптоматики центральной нервной системы и результатов исследований. Выписывают только с легким отклонением от нормы или вовсе в ее пределах. Фенобарбитал убирают постепенно, но обычно его пьют после выписки не менее 3 месяцев.